现在的位置:主页 > 综合新闻 >
川大万乾炳/王剑《自然·通讯》粘颊组织进行药
【作者】网站采编
【关键词】
【摘要】【科研摘要】 近年来,经由颊途径给药的药物引起了很多关注。但是,开发在潮湿条件下具有令人满意的粘附力和足够的药物生物利用度的系统仍然是一个挑战。最近,四川大学华西口
【科研摘要】
近年来,经由颊途径给药的药物引起了很多关注。但是,开发在潮湿条件下具有令人满意的粘附力和足够的药物生物利用度的系统仍然是一个挑战。最近,四川大学华西口腔医院万乾炳/王剑研究团队提出了以贻贝为灵感的粘膜粘膜。离体模型表明,该膜可对湿颊组织(高达38. kPa)具有较强的粘附力。证明了该膜的粘附机制依赖于膜和粘液之间的物理缔合和共价键。此外,掺有聚多巴胺纳米颗粒的薄膜在跨粘膜屏障运输方面显示出优越的优势,具有更高的药物生物利用度(比口服给药观察的约高3.5倍)和在口腔粘膜炎模型中的治疗功效(伤口闭合改善了约6.0倍)与第5天相比(未治疗)进行比较。我们预计,该平台可能有助于组织粘合剂的开发,并激发基于纳米颗粒的口腔给药系统的设计。相关论文以题为A mussel-inspired film for adhesion to wet buccal tissue and efficient buccal drug delivery发表在《Nature Communications》上。

【图文解析】
研究团队提出了一种颊粘膜组织粘合剂,其形式为可调谐薄膜,由粘膜粘附性聚合物聚乙烯醇(PVA)和贻贝粘附蛋白DOPA(PVA-DOPA膜)组合而成。离体猪和体内大鼠模型表明,该膜可与湿颊组织实现强粘附力和良好的机械匹配。团队还证明了薄膜的黏膜粘附强度和侵蚀速率与DOPA的量成正比。该膜的粘附机理依赖于膜与粘液之间的物理缔合和共价键。然后,采用三种聚合物,PEG,PVA,聚多巴胺(PDA),组装具有不同表面涂层的核-壳聚乳酸-乙醇酸(PLGA)NP(图1a),并将其掺入如图1b所示,PVA-DOPA薄膜形成一个组合的颊部药物递送系统(PVA-DOPA @ NPs薄膜)(NP指PLGA,PLGA-PEG,PLGA-PVA或PLGA-PDA NP)。通过系统评估,我们观察到PDA修饰的NPs表现出改善的粘液穿透能力和细胞摄取能力(图1c)。此外,与药物载有PLGA-PDA NP掺入的经颊给药的PVA-DOPA膜对口腔粘膜炎显示出最佳的生物利用度和优异的治疗功效。因此,我们提出了一个集成的颊部药物递送系统,其中NPs显示出受控的药物释放曲线,并改善了粘液穿透能力和细胞摄取,而屏蔽膜则显示出延长的停留时间和改善的粘膜粘附性。
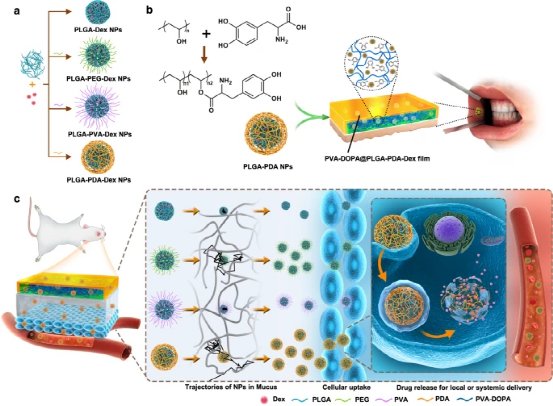
图1:PVA-DOPA @ NPs-Dex粘膜粘附膜的合成和生物医学应用。

图2:PVA-DOPA薄膜的特性和粘合强度。

图3:PVA-DOPA膜与粘蛋白的相互作用。
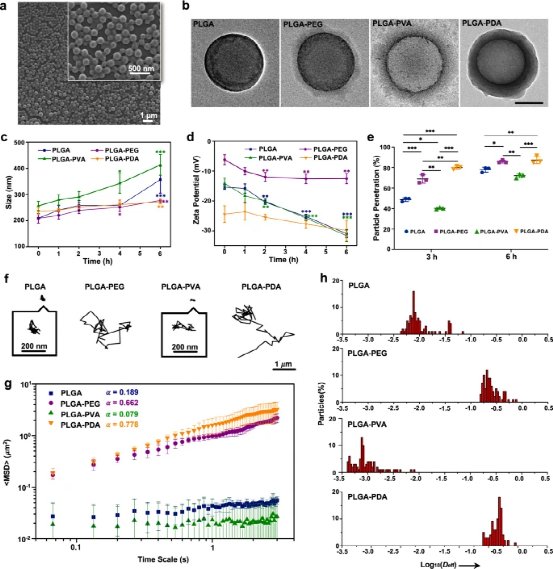
图4:体外NP的表征和粘液穿透特性。
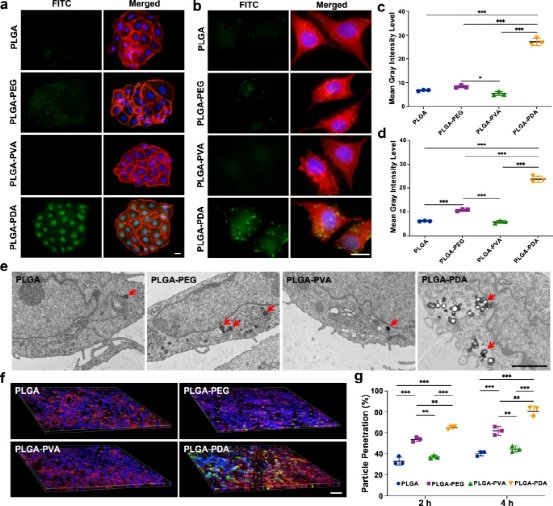
图5:NPs在体外的细胞吸收。

图6:离体和体内渗透研究。
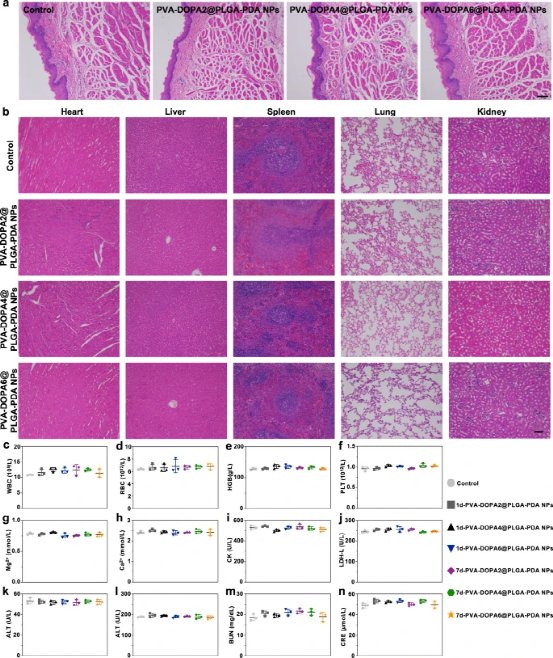
图7:体内生物安全性评估。
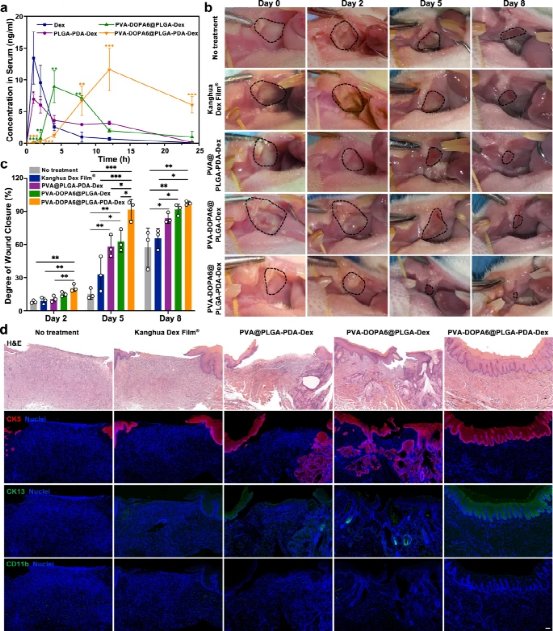
图8:PVA-DOPA @ NP膜在口腔溃疡中的体内药代动力学研究和治疗效果。
【总结】
在这项研究中,作者报道了一种生物启发性的粘膜粘附膜与NPs结合以改善粘膜粘附和药物的可获得性。这种复合粘膜粘附膜比以前的研究报道的材料具有优越的优势:(1)在口腔湿润环境中具有很强的粘附力,可以留出足够的停留时间;(2)薄膜形式的大小,厚度和腐蚀速率可调,以促进组织的机械匹配以及在需要不同剂量间隔的各种疾病中的潜在应用;(3)跨上皮屏障转运的能力;(4)控制和延长药物释放曲线。表1还总结了贻贝启发式PVA-DOPA @ NPs膜的粘膜粘附强度,跨粘膜屏障的转运效率,药物生物利用度和治疗功效,证明了其优势和通过颊途径在其他疾病中应用的潜力。
参考文献:doi.org/10.1038/s-021--5
文章来源:《化工设计通讯》 网址: http://www.hgsjtxzz.cn/zonghexinwen/2021/0321/647.html
化工设计通讯投稿 | 化工设计通讯编辑部| 化工设计通讯版面费 | 化工设计通讯论文发表 | 化工设计通讯最新目录
Copyright © 2018 《化工设计通讯》杂志社 版权所有
投稿电话: 投稿邮箱:


